近日,我组与海军军医大学药学系张磊教授合作,在酚酸类天然产物合成生物学研究方面取得新进展。在酿酒酵母中构建与优化了酚酸生物合成途径,强化了关键辅因子的供给和周转,实现了酚酸化合物的高效合成。
近年来,合成生物学快速发展使得天然产物可持续供应走向现实,在微生物细胞中构建完整生物合成途径,可实现系列复杂天然产物如青蒿酸、生物碱等的高效生物合成。酿酒酵母被广泛应用于食品酿造,且其具有极强的可塑性、鲁棒性和可靠的安全性,逐渐成为构建细胞工厂的主要平台之一。目前,虽然酶工程和途径工程已广泛应用于提高酵母细胞工厂的性能,但其用于合成天然产物的效率有待进一步提高。
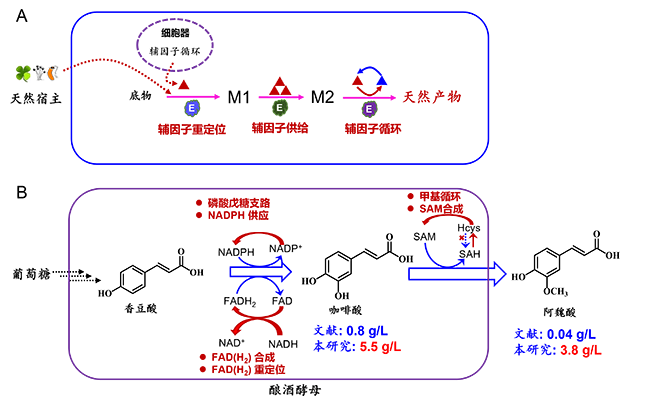
在上述背景下,合作团队致力于提升酚酸类天然产物合成效率。研究发现,细胞内辅因子参与的相关催化酶活性除了由酶表达量决定,还和辅因子水平有关,特别是表达外源酶时往往会面临辅因子不匹配或者供应不足的限制。由此,团队前期系统综述了辅因子在天然产物合成中的重要价值,并提供了四种可行的辅因子工程方案:重建辅因子的生物合成;提升胞内/细胞器内辅因子的代谢水平;平衡辅因子的稳态,以及提高辅因子的活性形式(iScience, 2020)。
酚酸化合物—咖啡酸在酵母中的生物合成需要辅因子FAD(H2)和NADPH,而阿魏酸的生物合成需要SAM作为甲基供体。本工作中,团队通过改造中心代谢以提高NADPH供应、构建胞浆FAD(H2)合成途径,以及将线粒体FAD(H2)导到胞浆以提高胞浆FAD(H2)供应等方式,显著提高了咖啡酸生物合成效率,使其产量达到5.5 g/L,远高于文献中已报道的0.8 g/L。在此基础上,团队利用高表达甲基转移酶,构建了阿魏酸生物合成途径,进一步强化了甲基循环以解除甲基转移酶抑制效应,提高了甲基供体辅因子SAM水平和SAM周转,使得阿魏酸产量达到3.8 g/L,远高于文献中已报道的0.04 g/L。该工作揭示了酵母中不同辅因子调控规律,特别是细胞内不同细胞器之间的辅因子分配规律,为辅因子调控提供了理论指导。并且,该工作将为复杂活性天然产物(木脂素和多聚酚酸等)的高效合成提供充足前体,有望为天然产物新资源开发和濒危中药资源的可持续利用提供保障。
相关研究成果以“Engineering cofactor supply and recycling to drive phenolic acid biosynthesis in yeast”为题,发表在《自然-化学生物学》(Nature Chemical Biology)上。该工作的第一作者是我组博士后陈瑞兵(已出站,现为海军军医大学副教授),瑞典查尔姆斯理工大学陈禹博士参与了代谢流分析工作。上述工作得到国家重点研究计划、国家自然科学基金面上项目、国家自然科学基金优秀青年基金、兴辽英才计划、我所科研创新基金等项目的资助。(文/图 陈瑞兵)
文章链接:https://doi.org/10.1038/s41589-022-01014-6
作者简介:
陈瑞兵,海军军医大学生药学博士(2015-2018),美国加州大学戴维斯分校联合培养博士(2017-2018),中国科学院大连化学物理研究所博士后(2019-2021),现为海军军医大学药学院军事药用植物学教研室副教授(2021-至今)。研究聚焦于合成生物学的军事应用和技术开发,围绕“保障打赢”的战略要求,致力于以合成生物学思维解决具有军事用途的中药活性成分合成和特殊作战环境威胁因子快速检测中的科学问题。获得国家自然科学基金青年基金项目和上海市“扬帆”计划资助,成果发表论文16篇,近五年以第一或共一作者在Nat Chem Biol、New Phytol、iScience、J. Exp. Bot.和Front. Plant Sci.等国际权威学术刊物发表论文9篇,总结出特色的仿生合成生物学策略指导天然产物合成,作为主要发明人申请国际和国内发明专利各2项,参编专著3部,作为负责人向国家农业农村部申请转基因黄花蒿中间试验批件3项。

